【单选】11.苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:
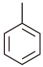
+KMnO
4→

+ MnO
2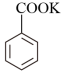
+HCl→
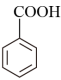
+KCl
| 名称 | 相对分
子质量 | 熔点/℃ | 沸点/℃ | 密度/(g·mL−1) | 溶解性 |
| 甲苯 | 92 | −95 | 110.6 | 0.867 | 不溶于水,易溶于乙醇 |
| 苯甲酸 | 122 | 122.4(100℃左右开始升华) | 248 | —— | 微溶于冷水,易溶于乙醇、热水 |
实验步骤:
(1)在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g(约0.03 mol)高锰酸钾,慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
(2)停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为1.0 g。
(3)纯度测定:称取0. 122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。每次移取25. 00 mL溶液,用0.01000 mol·L
−1的KOH标准溶液滴定,三次滴定平均消耗21. 50 mL的KOH标准溶液。
回答下列问题:
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为
______(填标号)。
A.100 mL
B.250 mL
C.500 mL D.1000 mL
(2)在反应装置中应选用
______冷凝管(填“直形”或“球形”),当回流液不再出现油珠即可判断反应已完成,其判断理由是
______。
(3)加入适量饱和亚硫酸氢钠溶液的目的是
___________;该步骤亦可用草酸在酸性条件下处理,请用反应的离子方程式表达其原理
__________。
(4)“用少量热水洗涤滤渣”一步中滤渣的主要成分是
_______。
(5)干燥苯甲酸晶体时,若温度过高,可能出现的结果是
_______。
(6)本实验制备的苯甲酸的纯度为
_______;据此估算本实验中苯甲酸的产率最接近于
_______(填标号)。
A.70%
B.60%
C.50% D.40%
(7)若要得到纯度更高的苯甲酸,可通过在水中
__________的方法提纯。
正确答案:B,您的答案:B,回答错误。
【解析】
Lorem ipsum dolor sit amet, consectetur adipiscing elit. Aenean euismod bibendum
laoreet. Proin gravida dolor sit amet lacus accumsan et viverra justo commodo. Proin
sodales pulvinar tempor. Cum sociis natoque penatibus et magnis dis parturient montes,
nascetur ridiculus mus. Nam fermentum, nulla luctus pharetra vulputate, felis tellus
mollis orci, sed rhoncus sapien nunc eget odio.