【单选】13.Fe、Co、Ni是三种重要的金属元素。回答下列问题:
(1)Fe、Co、Ni在周期表中的位置为
_________,基态Fe原子的电子排布式为
__________。
(2)CoO的面心立方晶胞如图所示。设阿伏加德罗常数的值为
NA,则CoO晶体的密度为
______g﹒cm
-3:三种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为
_______。

(3)Fe、Co、Ni能与Cl
2反应,其中Co和为Ni均生产二氯化物,由此推断FeCl
3、CoCl
3和Cl
2的氧化性由强到弱的顺序为
____,Co(OH)
3与盐酸反应有黄绿色气体生成,写出反应的离子方程式:
______。
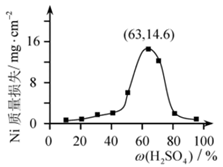
(4)95℃时,将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示,当

大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为
_____。由于Ni与H
2SO
4反应很慢,而与稀硝酸反应很快,工业上选用H
2SO
4和HNO
3的混酸与Ni反应制备NiSO
4。为了提高产物的纯度,在硫酸中添加HNO
3的方式为
______(填“一次过量”或“少量多次”),此法制备NiSO
4的化学方程式为
_______。
正确答案:B,您的答案:B,回答错误。
【解析】
Lorem ipsum dolor sit amet, consectetur adipiscing elit. Aenean euismod bibendum
laoreet. Proin gravida dolor sit amet lacus accumsan et viverra justo commodo. Proin
sodales pulvinar tempor. Cum sociis natoque penatibus et magnis dis parturient montes,
nascetur ridiculus mus. Nam fermentum, nulla luctus pharetra vulputate, felis tellus
mollis orci, sed rhoncus sapien nunc eget odio.