【单选】17.铁黄是一种重要的化工产品。由生产钛白粉废渣制备铁黄的过程如下。

资料:
i.钛白粉废渣成分:主要为FeSO
4·H
2O,含少量TiOSO
4和不溶物
ii.TiOSO
4+(x+1)H
2O
⇌TiO
2·xH
2O↓+H
2SO
4iii.0.1 mol/L Fe
2+生成Fe(OH)
2,开始沉淀时pH=6.3,完全沉淀时pH=8.3;
0.1 mol/L Fe
3+生成FeOOH,开始沉淀时pH=1.5,完全沉淀时pH=2.8
(1)纯化
①加入过量铁粉的目的是
_______。
②充分反应后,分离混合物的方法是
_______。
(2)制备晶种
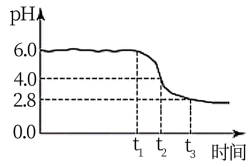
为制备高品质铁黄产品,需先制备少量铁黄晶种。过程及现象是:向一定浓度FeSO
4溶液中加入氨水,产生白色沉淀,并很快变成灰绿色。滴加氨水至pH为6.0时开始通空气并记录pH变化(如图)。
①产生白色沉淀的离子方程式是
_______。
②产生白色沉淀后的pH低于资料iii中的6.3。原因是:沉淀生成后c(Fe
2+)
_______0.1mol/L(填“>”“=”或“<”)。
③0-t
1时段,pH几乎不变;t
1-t
2时段,pH明显降低。结合方程式解释原因:
_______。
④pH≈4时制得铁黄晶种。若继续通入空气,t
3后pH几乎不变,此时溶液中c(Fe
2+)仍降低,但c(Fe
3+)增加,且(Fe
2+)降低量大于c(Fe
3+)增加量。结合总方程式说明原因:
_______。
(3)产品纯度测定
铁黄纯度可以通过产品的耗酸量确定。
wg铁黄

溶液b

溶液c

滴定
资料:Fe
3++3

=Fe(C
2O
4)

,Fe(C
2O
4)

不与稀碱液反应
Na
2C
2O
4过量,会使测定结果
_______(填“偏大”“偏小”或“不受影响”)。
正确答案:B,您的答案:B,回答错误。
【解析】
Lorem ipsum dolor sit amet, consectetur adipiscing elit. Aenean euismod bibendum
laoreet. Proin gravida dolor sit amet lacus accumsan et viverra justo commodo. Proin
sodales pulvinar tempor. Cum sociis natoque penatibus et magnis dis parturient montes,
nascetur ridiculus mus. Nam fermentum, nulla luctus pharetra vulputate, felis tellus
mollis orci, sed rhoncus sapien nunc eget odio.